職位推薦
- 珍格醫療-臨床銷售 15001-20000
- 地奧制藥-醫藥代表 6001-8000
- 普利德醫療-醫療設備銷售經理 面議
- 大唐-兼職招商經理 面議
- 景德中藥-直營經理 6001-8000
- 安邦醫藥-省區招商經理 8001-10000
- 恒瑞醫藥-醫藥信息溝通專員 6001-8000
- 黃河中藥-學術講師 8001-10000
發布日期:2025-09-03 瀏覽次數:415
近日,恒瑞醫藥收到國家藥品監督管理局的通知,批準公司自主研發的1類創新藥澤美妥司他片(商品名:艾瑞璟?)上市,用于既往接受過至少1線系統性治療的復發或難治外周T細胞淋巴瘤(R/R PTCL)成人患者。澤美妥司他片是中國首個自主研發的EZH2抑制劑,此次獲批彰顯了我國在血液腫瘤治療領域的新藥研發實力,將為R/R PTCL患者提供全新的治療選擇。
澤美妥司他片此次獲批是基于北京大學腫瘤醫院牽頭、全國多中心參與的關鍵性研究[1]。該結果表明,澤美妥司他片治療R/R PTCL患者完全緩解(CR)率達32.8%,意味著近三分之一的患者經治療后腫瘤病灶達到完全消失的狀態。同時,患者的中位PFS達到了10.0個月,展現出對疾病進展相對的有效控制。此外,客觀緩解率(ORR)為64.2%,中位緩解持續時間(DoR)為18.7個月,其療效廣泛覆蓋不同病理亞型[1]。
外周T細胞淋巴瘤(PTCL)是一組具有高度異質性和侵襲性的淋巴系統惡性腫瘤,在我國非霍奇金淋巴瘤患者中,其占比約25-30%[2],明顯高于西方國家;且患者中位發病年齡為52-57歲,也相對年輕[1,3-4]。PTCL臨床治療極具挑戰,多數患者在接受初始治療后復發或轉為難治[5]。近期一項覆蓋千余名中國患者的大型真實世界研究顯示,患者一旦進入二線治療,其中位無進展生存期(PFS)僅5.2個月,凸顯了R/R PTCL患者后續無統一的標準治療方案、治療手段匱乏、生存獲益微弱的困境[3,6]。
澤美妥司他片是恒瑞醫藥自主研發的一種高選擇性EZH2口服抑制劑,通過抑制組蛋白甲基轉移酶EZH2,抑制淋巴瘤細胞胞內H3K27Me3,逆轉腫瘤細胞的異常表觀遺傳編程,進而引起G1期細胞周期阻滯和誘導細胞早期凋亡,最終抑制淋巴瘤體外及體內生長[7]。這一獨特作用模式克服了傳統化療藥物及部分靶向療法的瓶頸,為R/R PTCL患者提供了全新的治療選擇。
作為創新型國際化制藥企業,恒瑞醫藥五十余年來始終踐行“科技為本,為人類創造健康生活”的使命,持續圍繞臨床亟需進行創新研發,目前已在中國獲批上市24款1類創新藥,其中抗腫瘤藥占比過半。另有100多個自主創新產品正在臨床開發,超400項臨床試驗在國內外開展。未來,恒瑞醫藥將持續“以患者為中心”加速創新研發步伐,致力于推出更多新藥好藥,服務健康中國,造福全球患者。
關于關鍵性研究
這是一項評估澤美妥司他在復發/難治性外周T細胞淋巴瘤患者中的單臂關鍵性研究[1]。該研究由北京大學腫瘤醫院朱軍教授、宋玉琴教授擔任主要研究者,全國33家中心共同參與。
該研究旨在評估澤美妥司他片單藥在R/R PTCL患者中的抗腫瘤療效和安全性。其主要研究終點為由獨立影像評審委員會(IRC)基于Lugano 2014標準評估的客觀緩解率(ORR),次要研究終點包括無進展生存期(PFS)、緩解持續時間(DoR)、總生存期(OS)等。
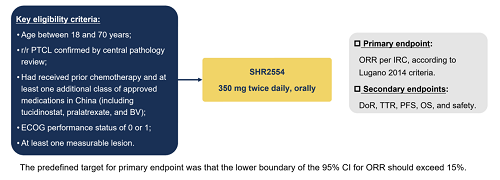
圖1.研究設計
該研究共納入67例R/R PTCL患者接受澤美妥司他片單藥治療(350mg,每日兩次)。結果表明,與歷史數據相比,澤美妥司他片取得了顯著且有臨床意義的改善,并展現出令人鼓舞的臨床數據:完全緩解(CR)率達32.8%,中位PFS為10.0個月。12個月和18個月的OS率分別達到了76.2%和74.3%。此外,部分緩解(PR)率為31.3%,ORR達64.2%,中位DoR為18.7個月。研究的安全性結果表明,澤美妥司他片耐受性良好,治療相關不良事件(TRAEs)多為低級別。
此外,不同組織學亞型的ORR均表現出較好的療效,如血管免疫母細胞性T細胞淋巴瘤(AITL)的ORR為70.3%,PTCL非特指型(PTCL-NOS)的ORR為57.1%,鼻型結外NK/T細胞淋巴瘤(ENKTL-NT)的ORR為50.0%,間變性大細胞淋巴瘤(ALCL,ALK-)的ORR為42.9%,ALCL(ALK+)的ORR為50.0%,單形性親上皮性腸道T細胞淋巴瘤(MEITL)及其他亞型的ORR均為100%。
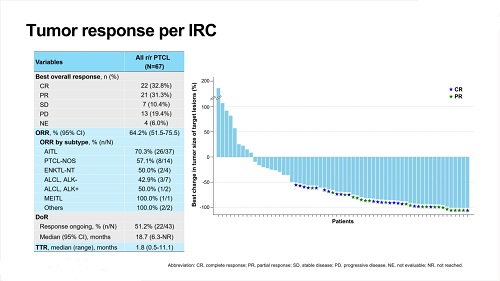
圖2.研究結果
目前,一項比較澤美妥司他與西達本胺治療R/R PTCL的隨機對照III期研究正在進行中(ClinicalTrials.gov,NCT06122389),有望在未來進一步驗證澤美妥司他的療效和安全性,為臨床醫生提供更充分的循證醫學證據,推動PTCL治療領域的發展。
參考文獻:
[1] SONG Y, LI Z, JIN Z, et al. A PIVOTAL STUDY OF SHR2554, AN ORAL INHIBITOR AGAINST ENHANCER OF ZESTE HOMOLOG 2 (EZH2), IN RELAPSED OR REFRACTORY (R/R) PERIPHERAL T-CELL LYMPHOMA (PTCL) [J]. Hematological Oncology, 2025, 43(S3): e61_70093.
[2]SUN J, YANG Q, LU Z, et al. Distribution of lymphoid neoplasms in China: analysis of 4,638 cases according to the World Health Organization classification [J]. Am J Clin Pathol, 2012, 138(3): 429-34.
[3]HUANG L, YANG Y, ZHAO Z, et al. Clinical characteristics, treatment patterns, and survival outcomes of 1031 patients with peripheral T cell lymphoma in china: a multicenter, real-world study [J]. Discov Oncol, 2025, 16(1): 1252.
[4] YOON S E, SONG Y, KIM S J, et al. Comprehensive analysis of peripheral T-cell and natural killer/T-cell lymphoma in Asian patients: A multinational, multicenter, prospective registry study in Asia[J]. Lancet Reg Health West Pac, 2021, 10: 100126.
[5]LUAN Y, LI X, LUAN Y, et al. Therapeutic challenges in peripheral T-cell lymphoma [J]. Mol Cancer, 2024, 23(1): 2.
[6]復發難治外周T細胞淋巴瘤治療進展;白血病·淋巴瘤, 2022,31(10) : 634-637. DOI: 10.3760/cma.j.cn115356-20210904-00207.
[7]GULATI N, BéGUELIN W, GIULINO-ROTH L. Enhancer of zeste homolog 2 (EZH2) inhibitors [J]. Leuk Lymphoma, 2018, 59(7): 1574-85.
聲明:
1.本新聞旨在分享研發注冊進展信息,僅供醫療衛生專業人士參閱,非廣告用途。
2.恒瑞醫藥不對任何藥品和/或適應癥作推薦。
3.本新聞中涉及的信息僅供參考,請遵從醫生或其他醫療衛生專業人士的意見或指導。醫療衛生專業人士作出的任何與治療有關的決定應根據患者的具體情況并遵照藥品說明書。
300多萬優質簡歷
17年行業積淀
2萬多家合作名企業

微信掃一掃 使用小程序

